肺高血圧症治療ガイドライン(2012年改訂版)
Guidelines for Treatment of Pulmonary Hypertension(JCS2012)
Guidelines for Treatment of Pulmonary Hypertension(JCS2012)
Class Ⅰ
心不全治療ガイドラインに基づいた心不全自体の治療
(エビデンスLevel C)
弁膜症治療ガイドラインに基づいた弁膜症の治療
(エビデンスLevel C)
Class Ⅱb
運動耐容能およびQOL 改善を目的としたシルデナフィル
(エビデンスLevel B)
Class Ⅲ
予後改善を目的としたエポプロステノール
(エビデンスLevel C)
予後改善を目的としたボセンタン
(エビデンスLevel C)
心不全治療ガイドラインに基づいた心不全自体の治療
(エビデンスLevel C)
弁膜症治療ガイドラインに基づいた弁膜症の治療
(エビデンスLevel C)
Class Ⅱb
運動耐容能およびQOL 改善を目的としたシルデナフィル
(エビデンスLevel B)
Class Ⅲ
予後改善を目的としたエポプロステノール
(エビデンスLevel C)
予後改善を目的としたボセンタン
(エビデンスLevel C)
さらなる肺動脈圧の上
昇と可逆性の消失
左室収縮機能不全左室拡張機能不全
左室充満圧障害
僧帽弁狭窄症
左房粘液腫瘍
左室流入障害
左房圧上昇
肺動脈圧上昇
肺動脈収縮および
リモデリング
昇と可逆性の消失
左室収縮機能不全左室拡張機能不全
左室充満圧障害
僧帽弁狭窄症
左房粘液腫瘍
左室流入障害
左房圧上昇
肺動脈圧上昇
肺動脈収縮および
リモデリング
2 左心疾患による肺高血圧症
要旨
肺高血圧症例の中で,肺静脈圧の上昇が原因となる肺高血圧症は,ダナポイント分類では左心疾患による肺高血圧症と命名された.本症の症例数は肺高血圧症の中で一番多いと想定され,さらに左室の収縮不全,拡張不全,弁膜症の3群に亜分類され,ニース会議では,これに先天性/後天性の左心流入路/流出路閉塞が追加された.これらの左心不全による肺高血圧症の予後は不良であることが知られているが,疫学情報は現在も十分ではない.左心疾患による肺高血圧症では,肺高血圧症は存在するが,肺動脈楔入圧も高いため,計算上の肺血管抵抗は低いものの一部の例で肺血管抵抗が著明に上昇していることがある.左心疾患による肺高血圧症に対する治療は,その原疾患に対する治療が優先される.本症に対するPAH治療薬の臨床試験では,十分な治療効果は得られていない.
①機序
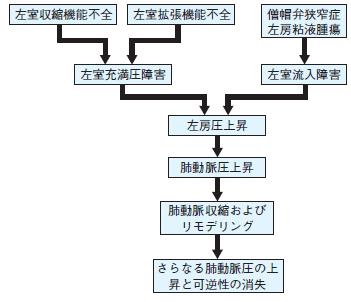
様々な左心疾患により肺静脈性肺高血圧がもたらされる.肺静脈性肺高血圧の原因となる左心疾患はまず左心不全をはじめとする左室充満圧の上昇を来たす疾患,僧房弁狭窄症や左房粘液腫のように左室の流入が障害され左房圧の上昇を来たす疾患などがある.左心疾患による肺高血圧の作用機序を図10に示した216).
まず,左心不全は左室収縮機能の低下に基づく心不全と左室収縮機能の保持された心不全に分けられるが,原因にかかわらず左室充満圧は上昇し,その結果左房圧も上昇する.僧房弁狭窄症や左房粘液種では,左室への血液流入障害があるため左室充満圧の上昇はないが,やはり左房圧は上昇する.上昇した左房圧は肺静脈から肺毛細血管を介して肺動脈系に伝搬され,肺動脈圧は上昇する.この段階では肺高血圧は可逆性で,治療により左房圧が下がれば肺動脈圧も低下する.しかしこの状態が長期にわたり持続すると,肺動脈の反応性収縮が起こり肺高血圧が悪化する.さらには肺動脈のリモデリングが起こり解剖学的変化を来たすと,肺高血圧はさらに進行し,肺高血圧はもはや不可逆性となってしまう.このような状態は以前は“out of proportion”,つまり,肺静脈圧の上昇では説明のできないほどの肺高血圧を来たした状態と言われ,原疾患の治療を行っても肺高血圧は改善せず,弁置換後,心臓移植後の右心不全につながってゆく.
左房圧の上昇を来たす左心疾患のうち,収縮性心膜炎では例外的に肺動脈圧の上昇は肺静脈圧を反映しない.収縮性心膜炎では右心系の充満圧も左心系と同様に上昇するため,左心系充満圧の肺動脈への伝搬は起こらない.また1回拍出量の低下に伴い右室の発生圧は低いため,右室拡張期圧+右室発生圧で決定される肺動脈収縮期圧は上昇しない.
②疫学,原因
肺高血圧症全体の原因として最も多いものは,実は左心疾患に起因する肺静脈性肺高血圧である.我が国における明らかな統計はないが,欧米の統計では左心機能不全患者の26~ 80%に肺高血圧を合併すると報告されている217)-219).我が国の心不全患者は100万人を超えると推定され,そのほとんどが左心不全であることを考慮すると,肺静脈性肺高血圧を伴う患者数は実はPAH患者数をはるかにしのぐ.最近増加している,左室収縮機能の保持された心不全(拡張期心不全または拡張性心不全)においても,肺高血圧症は高頻度に合併する219),220).自治医科大学さいたま医療センターに2010年に心不全で入院した患者計125名のうち,心エコーデータの揃っている99名の解析では 収縮機能の低下した(LVEF<40%,n= 67)心不全患者の43%,左室収縮機能の保持された(LVEF> 40 %,n= 32)50 % に推定肺動脈収縮期圧35mmHg以上の肺高血圧がみられている.
さらに肺高血圧は,心不全の予後悪化要因であることも1992年のAbramson の報告以来多くの研究によって明らかにされている217),218),221).過去の多くの報告は左室収縮機能の低下による心不全についてのものであったが,左室収縮機能の保持された心不全においてもやはり不良な予後の予測因子であることがLamによって最近報告され219)注目を集めている.
本群に属する肺高血圧症例の疫学については,まだ十分な資料はない.左心不全による心臓移植待機患者では,肺血管抵抗> 3.5 Wood単位を肺高血圧症とすると,その頻度は19~ 35%との報告がある222),223).また別の報告では28か月の追跡期間で,中等度の肺高血圧合併例の死亡率は57%であったのに比して,肺高血圧非合併の心不全例では17%であった224).心不全例で肺高血圧合併例の予後は不良と報告されている.
③診断方法
左室収縮機能低下に基づく心不全および左室拡張機能障害に基づく心不全の診断については『慢性心不全治療ガイドライン(2010年改訂版)』(慢性心不全治療ガイドライン)を参照されたいが,要約すると左室収縮機能低下に基づく心不全は心エコーなどで比較的診断が容易であるが,しばしば診断に困るのは左室収縮機能の保持された,つまり左室拡張機能障害に基づく心不全である.このタイプの心不全の診断はまず症状やBNPから心不全が疑われるが,左室駆出率が40~ 50%以上であることから始まる.この中から心不全と類似の非心臓疾患を除外したのち,先天性心疾患,心臓弁膜症,高拍出性心不全,心膜疾患,そしてPAHなどの基礎心疾患を除外した上で,心エコー・ドプラー検査における拡張期左室血液流入パターン,肺静脈環流パターン,および僧帽弁輪組織ドップラー,左房径または左房容積,BNP(またはNT-Pro BNP),右心カテーテルで実測した肺動脈楔入圧などから拡張機能障害の診断を確定してゆくことが推奨されている.
左心疾患による肺高血圧のほとんどは肺静脈圧の上昇に見合った程度のものであるが,なかには左心不全に伴う肺静脈圧の上昇のみでは説明しきれないほどの肺高血圧つまり“out of proportion”の肺高血圧を有する左心不全患者が存在する. 肺静脈性肺高血圧ではtranspulmonary pressure gradient(TPG: 平均肺動脈圧─平均肺動脈楔入圧) は12mmHg を超えない.TPGが12mmHgを超える場合には肺動脈そのものに起因するPAHの要素が加わっていると考えられる.このような
TPG上昇例は心不全に対する一般的治療に応じた肺動脈圧の低下が得られなかったり,心臓移植術後の右心不全の遷延さらには予後の悪化につながることなどから問題となる.過去の報告をみるとPVR> 2.5 Wood unit ,TPG> 15mmHgは術後の不良な予後の予測因子と考えられる225)-228).一方ニトロプルシドなど血管拡張薬に対する血管反応性試験により,PVRが2.5 Wood unit以下となる症例では移植後の予後が良好であるとの報告もある223).右心カテーテルによる肺血管拡張試験は左心疾患に基づく肺高血圧に対してはルーチン検査として推奨されないが,心臓移植術前患者においては,上記のように予後予測にある程度有効であるので推奨されている.
なお我が国の心臓移植の適応基準の除外条件として肺高血圧症(肺血管抵抗が血管拡張薬を使用しても6Wood単位以上)が挙げられている(日本循環器学会心
臓移植委員会.心臓移植の適応. http://plaza.umin.ac.jp/~hearttp/).
④治療(表28)
左心疾患による肺高血圧を是正するためにはまず原因となっている左心疾患の治療が先決である.左室機能不全が原因と考えられる場合には慢性心不全治療ガイドラインに準拠した心機能不全の治療が優先される.左室収縮機能不全に基づく心不全がある場合にはうっ血を軽減するための利尿薬,予後改善を目的としたACE阻害薬(ACE阻害薬に忍容性がない場合にはARB),β 遮断薬,アルドステロン拮抗薬(NYHAⅢ度以上の心不全がある場合)である.非薬物治療としてはCRT,ICD,和温療法,合併する睡眠呼吸障害治療,心臓移植などが推奨される.利尿薬による短期的な水分,Na 貯留の是正とエビデンスに基づいた心保護薬や非薬物療法による左室リモデリングの逆行は,左室充満圧を低下し肺動脈圧の低下をもたらす.左室拡張機能不全基づく心不全においては,うっ血を軽減し左室充満圧を下げるためにはやはり利尿薬が必要であるが,予後自体を改善する薬剤は未だ明らかとなっていない.
僧帽弁狭窄症をはじめとする弁膜症,左房粘液腫に対してはそれぞれのガイドラインなどの治療指針に従ったPTMC,弁形成術,弁置換術が適応される.弁膜症における肺高血圧の合併は,自覚症状の有無にかかわらず病態の進行を意味し,ガイドラインにおいて積極的治療が推奨されている(循環器病の診断と治療に関するガイドライン[2006年度合同研究班報告]弁膜疾患の非薬物治療に関するガイドライン[2007年改訂版]).一般にPTMC,弁置換術などの治療に伴い,僧帽弁狭窄症患者の肺動脈圧は低下する229)-233)が,肺動脈系に解剖学的変化を来たしている症例ではPAHの要素が加わり術後も肺高血圧が持続することがあることは古くから知られている234),235).
⑤ 左心疾患による肺高血圧に対する肺動脈性肺高血圧治療薬の治療
肺高血圧を伴う心不全患者を対象としたPAH治療薬の臨床試験では,あまり目立った成果は得られていない.例えばプロスタノイドであるエポプロステロールを用い
たFIRST試験ではNYHAⅢb/Ⅳの左室収縮機能低下に基づく比較的重症心不全患者が対象となり,血行動態は改善したものの予後は悪化する傾向にあり早期に打ち切られた236).またエンドセリン受容体拮抗薬については,Reach 1試験では,やはりNYHAⅢB/Ⅳ度心不全患者が対象のボセンタンとプラセボの比較が行われたが,ボセンタンの肝障害のために早期中止となった237).300名の重症心不全患者を対象としたEnable 1 試験では,ボセンタンの目的用量1日500mg 投与で開始後1 か月目の心不全の悪化は増加傾向にあり238),Enable 2試験ではさらに症例数を増やし(1,613人),ボセンタンの目標用量も1日250mgに減量されたが,一次エンドポイントである総死亡または入院は減少せずむしろ早期の心不全悪化による入院が増加した239).他のエンドセリン拮抗薬については,急性非代償性左心不全を対象とする静注enresentanを用いたEncor試験では,血行動態の改善は得られたが有害事象が増加し240),NYHA Class は悪化の傾向を示し,darusentanのEARTH試験では左室リモデリング,入院,死亡率に対する改善効果は示されなかった241).
一方NO-cGMPシグナル伝達系に作用する薬剤についての臨床試験も行われている.Lewisらは小数例でシルデナフィルが心不全患者の運動耐容能を改善することを報告している242).Behlingも1 か月のシルデナフィル投与でpeak VO2 が21%改善したと報告している243).最近ではGuazzらがNYHAⅡ度,Ⅲ度の心不全患者45名で,1日150mgのシルデナフィル投与により運動耐容能のみならず拡張機能も改善することを報告している244).しかしながら,PDE 5阻害薬が左心不全患者の臨床アウトカムを改善するかどうかについては未だ明らかになっていない.一方,cinaciguatをはじめとする可溶性グアニル酸シクラーゼの刺激薬や,活性化薬も左心疾患による肺高血圧症に試みられている.僧帽弁術後の遷延する肺高血圧にも肺動脈拡張薬を試みた報告があり245),Trachteらは小数例の肺高血圧を伴う弁膜症術後患者にシルデナフィルを用いて有効であったと報告している246).
いわゆるout of proportion症例については,このような肺動脈拡張作用を有する薬剤は有効である可能性があるが,肺高血圧を伴う左心不全全体についてみると,明確なエビデンスは未だ構築されていない状況である.今後さらに肺血管収縮を軽減する薬剤の心不全治療への可能性が検討されるべきで,そのためには綿密に計画され,臨床アウトカムを指標とした臨床試験が必要である.
肺高血圧症例の中で,肺静脈圧の上昇が原因となる肺高血圧症は,ダナポイント分類では左心疾患による肺高血圧症と命名された.本症の症例数は肺高血圧症の中で一番多いと想定され,さらに左室の収縮不全,拡張不全,弁膜症の3群に亜分類され,ニース会議では,これに先天性/後天性の左心流入路/流出路閉塞が追加された.これらの左心不全による肺高血圧症の予後は不良であることが知られているが,疫学情報は現在も十分ではない.左心疾患による肺高血圧症では,肺高血圧症は存在するが,肺動脈楔入圧も高いため,計算上の肺血管抵抗は低いものの一部の例で肺血管抵抗が著明に上昇していることがある.左心疾患による肺高血圧症に対する治療は,その原疾患に対する治療が優先される.本症に対するPAH治療薬の臨床試験では,十分な治療効果は得られていない.
①機序
様々な左心疾患により肺静脈性肺高血圧がもたらされる.肺静脈性肺高血圧の原因となる左心疾患はまず左心不全をはじめとする左室充満圧の上昇を来たす疾患,僧房弁狭窄症や左房粘液腫のように左室の流入が障害され左房圧の上昇を来たす疾患などがある.左心疾患による肺高血圧の作用機序を図10に示した216).
まず,左心不全は左室収縮機能の低下に基づく心不全と左室収縮機能の保持された心不全に分けられるが,原因にかかわらず左室充満圧は上昇し,その結果左房圧も上昇する.僧房弁狭窄症や左房粘液種では,左室への血液流入障害があるため左室充満圧の上昇はないが,やはり左房圧は上昇する.上昇した左房圧は肺静脈から肺毛細血管を介して肺動脈系に伝搬され,肺動脈圧は上昇する.この段階では肺高血圧は可逆性で,治療により左房圧が下がれば肺動脈圧も低下する.しかしこの状態が長期にわたり持続すると,肺動脈の反応性収縮が起こり肺高血圧が悪化する.さらには肺動脈のリモデリングが起こり解剖学的変化を来たすと,肺高血圧はさらに進行し,肺高血圧はもはや不可逆性となってしまう.このような状態は以前は“out of proportion”,つまり,肺静脈圧の上昇では説明のできないほどの肺高血圧を来たした状態と言われ,原疾患の治療を行っても肺高血圧は改善せず,弁置換後,心臓移植後の右心不全につながってゆく.
左房圧の上昇を来たす左心疾患のうち,収縮性心膜炎では例外的に肺動脈圧の上昇は肺静脈圧を反映しない.収縮性心膜炎では右心系の充満圧も左心系と同様に上昇するため,左心系充満圧の肺動脈への伝搬は起こらない.また1回拍出量の低下に伴い右室の発生圧は低いため,右室拡張期圧+右室発生圧で決定される肺動脈収縮期圧は上昇しない.
②疫学,原因
肺高血圧症全体の原因として最も多いものは,実は左心疾患に起因する肺静脈性肺高血圧である.我が国における明らかな統計はないが,欧米の統計では左心機能不全患者の26~ 80%に肺高血圧を合併すると報告されている217)-219).我が国の心不全患者は100万人を超えると推定され,そのほとんどが左心不全であることを考慮すると,肺静脈性肺高血圧を伴う患者数は実はPAH患者数をはるかにしのぐ.最近増加している,左室収縮機能の保持された心不全(拡張期心不全または拡張性心不全)においても,肺高血圧症は高頻度に合併する219),220).自治医科大学さいたま医療センターに2010年に心不全で入院した患者計125名のうち,心エコーデータの揃っている99名の解析では 収縮機能の低下した(LVEF<40%,n= 67)心不全患者の43%,左室収縮機能の保持された(LVEF> 40 %,n= 32)50 % に推定肺動脈収縮期圧35mmHg以上の肺高血圧がみられている.
さらに肺高血圧は,心不全の予後悪化要因であることも1992年のAbramson の報告以来多くの研究によって明らかにされている217),218),221).過去の多くの報告は左室収縮機能の低下による心不全についてのものであったが,左室収縮機能の保持された心不全においてもやはり不良な予後の予測因子であることがLamによって最近報告され219)注目を集めている.
本群に属する肺高血圧症例の疫学については,まだ十分な資料はない.左心不全による心臓移植待機患者では,肺血管抵抗> 3.5 Wood単位を肺高血圧症とすると,その頻度は19~ 35%との報告がある222),223).また別の報告では28か月の追跡期間で,中等度の肺高血圧合併例の死亡率は57%であったのに比して,肺高血圧非合併の心不全例では17%であった224).心不全例で肺高血圧合併例の予後は不良と報告されている.
③診断方法
左室収縮機能低下に基づく心不全および左室拡張機能障害に基づく心不全の診断については『慢性心不全治療ガイドライン(2010年改訂版)』(慢性心不全治療ガイドライン)を参照されたいが,要約すると左室収縮機能低下に基づく心不全は心エコーなどで比較的診断が容易であるが,しばしば診断に困るのは左室収縮機能の保持された,つまり左室拡張機能障害に基づく心不全である.このタイプの心不全の診断はまず症状やBNPから心不全が疑われるが,左室駆出率が40~ 50%以上であることから始まる.この中から心不全と類似の非心臓疾患を除外したのち,先天性心疾患,心臓弁膜症,高拍出性心不全,心膜疾患,そしてPAHなどの基礎心疾患を除外した上で,心エコー・ドプラー検査における拡張期左室血液流入パターン,肺静脈環流パターン,および僧帽弁輪組織ドップラー,左房径または左房容積,BNP(またはNT-Pro BNP),右心カテーテルで実測した肺動脈楔入圧などから拡張機能障害の診断を確定してゆくことが推奨されている.
左心疾患による肺高血圧のほとんどは肺静脈圧の上昇に見合った程度のものであるが,なかには左心不全に伴う肺静脈圧の上昇のみでは説明しきれないほどの肺高血圧つまり“out of proportion”の肺高血圧を有する左心不全患者が存在する. 肺静脈性肺高血圧ではtranspulmonary pressure gradient(TPG: 平均肺動脈圧─平均肺動脈楔入圧) は12mmHg を超えない.TPGが12mmHgを超える場合には肺動脈そのものに起因するPAHの要素が加わっていると考えられる.このような
TPG上昇例は心不全に対する一般的治療に応じた肺動脈圧の低下が得られなかったり,心臓移植術後の右心不全の遷延さらには予後の悪化につながることなどから問題となる.過去の報告をみるとPVR> 2.5 Wood unit ,TPG> 15mmHgは術後の不良な予後の予測因子と考えられる225)-228).一方ニトロプルシドなど血管拡張薬に対する血管反応性試験により,PVRが2.5 Wood unit以下となる症例では移植後の予後が良好であるとの報告もある223).右心カテーテルによる肺血管拡張試験は左心疾患に基づく肺高血圧に対してはルーチン検査として推奨されないが,心臓移植術前患者においては,上記のように予後予測にある程度有効であるので推奨されている.
なお我が国の心臓移植の適応基準の除外条件として肺高血圧症(肺血管抵抗が血管拡張薬を使用しても6Wood単位以上)が挙げられている(日本循環器学会心
臓移植委員会.心臓移植の適応. http://plaza.umin.ac.jp/~hearttp/).
④治療(表28)
左心疾患による肺高血圧を是正するためにはまず原因となっている左心疾患の治療が先決である.左室機能不全が原因と考えられる場合には慢性心不全治療ガイドラインに準拠した心機能不全の治療が優先される.左室収縮機能不全に基づく心不全がある場合にはうっ血を軽減するための利尿薬,予後改善を目的としたACE阻害薬(ACE阻害薬に忍容性がない場合にはARB),β 遮断薬,アルドステロン拮抗薬(NYHAⅢ度以上の心不全がある場合)である.非薬物治療としてはCRT,ICD,和温療法,合併する睡眠呼吸障害治療,心臓移植などが推奨される.利尿薬による短期的な水分,Na 貯留の是正とエビデンスに基づいた心保護薬や非薬物療法による左室リモデリングの逆行は,左室充満圧を低下し肺動脈圧の低下をもたらす.左室拡張機能不全基づく心不全においては,うっ血を軽減し左室充満圧を下げるためにはやはり利尿薬が必要であるが,予後自体を改善する薬剤は未だ明らかとなっていない.
僧帽弁狭窄症をはじめとする弁膜症,左房粘液腫に対してはそれぞれのガイドラインなどの治療指針に従ったPTMC,弁形成術,弁置換術が適応される.弁膜症における肺高血圧の合併は,自覚症状の有無にかかわらず病態の進行を意味し,ガイドラインにおいて積極的治療が推奨されている(循環器病の診断と治療に関するガイドライン[2006年度合同研究班報告]弁膜疾患の非薬物治療に関するガイドライン[2007年改訂版]).一般にPTMC,弁置換術などの治療に伴い,僧帽弁狭窄症患者の肺動脈圧は低下する229)-233)が,肺動脈系に解剖学的変化を来たしている症例ではPAHの要素が加わり術後も肺高血圧が持続することがあることは古くから知られている234),235).
⑤ 左心疾患による肺高血圧に対する肺動脈性肺高血圧治療薬の治療
肺高血圧を伴う心不全患者を対象としたPAH治療薬の臨床試験では,あまり目立った成果は得られていない.例えばプロスタノイドであるエポプロステロールを用い
たFIRST試験ではNYHAⅢb/Ⅳの左室収縮機能低下に基づく比較的重症心不全患者が対象となり,血行動態は改善したものの予後は悪化する傾向にあり早期に打ち切られた236).またエンドセリン受容体拮抗薬については,Reach 1試験では,やはりNYHAⅢB/Ⅳ度心不全患者が対象のボセンタンとプラセボの比較が行われたが,ボセンタンの肝障害のために早期中止となった237).300名の重症心不全患者を対象としたEnable 1 試験では,ボセンタンの目的用量1日500mg 投与で開始後1 か月目の心不全の悪化は増加傾向にあり238),Enable 2試験ではさらに症例数を増やし(1,613人),ボセンタンの目標用量も1日250mgに減量されたが,一次エンドポイントである総死亡または入院は減少せずむしろ早期の心不全悪化による入院が増加した239).他のエンドセリン拮抗薬については,急性非代償性左心不全を対象とする静注enresentanを用いたEncor試験では,血行動態の改善は得られたが有害事象が増加し240),NYHA Class は悪化の傾向を示し,darusentanのEARTH試験では左室リモデリング,入院,死亡率に対する改善効果は示されなかった241).
一方NO-cGMPシグナル伝達系に作用する薬剤についての臨床試験も行われている.Lewisらは小数例でシルデナフィルが心不全患者の運動耐容能を改善することを報告している242).Behlingも1 か月のシルデナフィル投与でpeak VO2 が21%改善したと報告している243).最近ではGuazzらがNYHAⅡ度,Ⅲ度の心不全患者45名で,1日150mgのシルデナフィル投与により運動耐容能のみならず拡張機能も改善することを報告している244).しかしながら,PDE 5阻害薬が左心不全患者の臨床アウトカムを改善するかどうかについては未だ明らかになっていない.一方,cinaciguatをはじめとする可溶性グアニル酸シクラーゼの刺激薬や,活性化薬も左心疾患による肺高血圧症に試みられている.僧帽弁術後の遷延する肺高血圧にも肺動脈拡張薬を試みた報告があり245),Trachteらは小数例の肺高血圧を伴う弁膜症術後患者にシルデナフィルを用いて有効であったと報告している246).
いわゆるout of proportion症例については,このような肺動脈拡張作用を有する薬剤は有効である可能性があるが,肺高血圧を伴う左心不全全体についてみると,明確なエビデンスは未だ構築されていない状況である.今後さらに肺血管収縮を軽減する薬剤の心不全治療への可能性が検討されるべきで,そのためには綿密に計画され,臨床アウトカムを指標とした臨床試験が必要である.
図10 左心疾患に伴う肺高血圧症の発症機序
表28 左心疾患に伴う肺高血圧症の治療
Ⅱ 各論 >
2 左心疾患による肺高血圧症